私たちの体内には、生命を維持するために不可欠な二つの重要な循環系が存在しています。心臓から全身に血液を送り届け、酸素や栄養素を運搬する血管系と、組織から老廃物や余分な水分を回収するリンパ管系です。これらは互いに密接に関連しながらも、通常の状態では決して混ざり合うことのない独立した存在として機能しています。しかし、なぜこの二つの系統は独立性を保つことができるのでしょうか。長年、医学界ではこのメカニズムの解明が重要な課題とされてきました。2020年12月、熊本大学と慶應義塾大学の研究チームによって、この謎を解く画期的な最新研究が国際的権威のある科学雑誌Nature Communicationsに発表されました。この発見は、血管とリンパ管の独立性を維持する分子レベルでの制御機構を明らかにし、リンパ浮腫やがん治療など、さまざまな疾患の新しい治療法開発への道を開く可能性を秘めています。本記事では、この革新的な研究成果と、それが医療にもたらす未来について詳しく解説していきます。
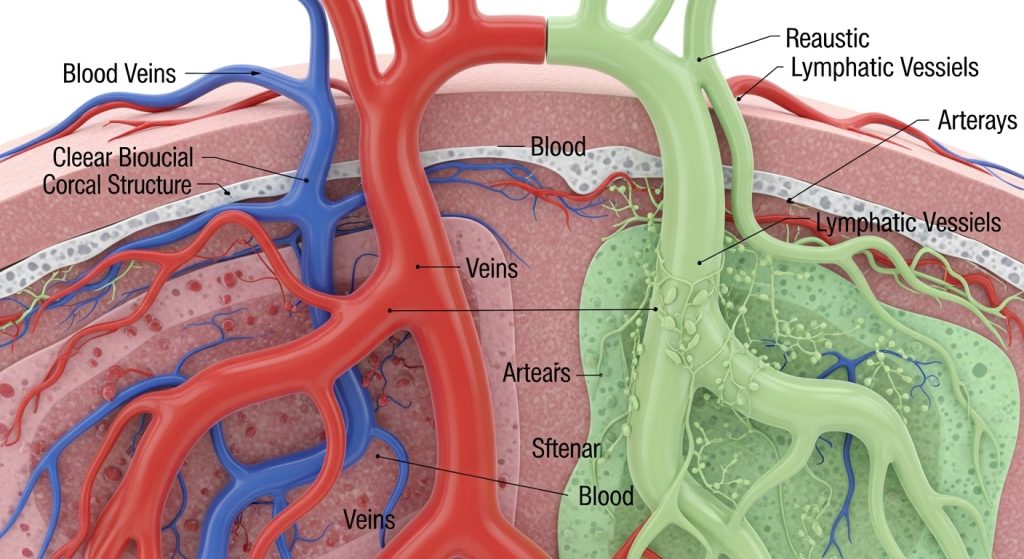
血管とリンパ管が持つ異なる役割と独立性の重要性
人体における血管系は、心臓という強力なポンプによって駆動される閉鎖的な循環システムです。動脈を通じて酸素や栄養素を含んだ血液が全身の組織に送り届けられ、静脈を通じて二酸化炭素や老廃物を含んだ血液が心臓に戻ってきます。この循環は休むことなく続き、私たちの生命活動を支えています。血管、特に毛細血管は比較的密な構造を持ち、血液成分が不必要に漏れ出さないように設計されています。
一方、リンパ管系は、血管系とは異なる独特の機能を持っています。リンパ管は心臓のようなポンプを持たず、筋肉の収縮や呼吸運動などによる外部からの圧力によってリンパ液が流れています。毛細リンパ管は片方が閉じた盲端構造を持ち、内皮細胞間の接着が緩く、組織液を容易に取り込めるようになっています。この構造により、リンパ管は血管から漏れ出た組織液を効率的に回収し、最終的には鎖骨下静脈に戻すことで、体液のバランスを維持しています。
これら二つの系統が独立性を保つことは、生命維持にとって極めて重要です。もし血管とリンパ管が異常に接続してしまうと、血圧の高い血管からリンパ管に血液が逆流し、リンパ系の機能が破綻してしまう可能性があります。通常、これら二つの系統は胎児の発生段階から成体に至るまで、厳密に分離された状態を維持していますが、その独立性を維持するメカニズムについては長年謎とされてきました。
FLCN遺伝子による独立性維持メカニズムの画期的解明
最新研究により、この謎を解く鍵となる分子が発見されました。それがFLCN(フォリクリン)という遺伝子です。熊本大学と慶應義塾大学の研究チームは、遺伝子改変マウスを用いた精密な実験により、FLCNが血管とリンパ管の独立性を守る「門番」のような役割を果たしていることを明らかにしました。
研究チームは、血管内皮細胞において特異的にFLCNを欠損させるという実験を行いました。その結果、驚くべき現象が観察されました。通常では決して接続しないはずの血管とリンパ管が異常に吻合してしまったのです。この発見は、FLCNが血管内皮細胞において、リンパ管との分離を維持するために不可欠な役割を担っていることを示しています。
FLCNという遺伝子は、元々バート・ホッグ・デューベ症候群という遺伝性疾患の原因遺伝子として同定されていました。この疾患では、皮膚の良性腫瘍、肺嚢胞、腎臓がんなどが発症しやすくなることが知られていました。FLCNは細胞増殖やエネルギー代謝の制御に関わることが以前から報告されていましたが、今回の最新研究により、血管とリンパ管のメカニズムにおける新たな重要な機能が解明されたことになります。
この発見の重要性は、単に一つの遺伝子の機能を明らかにしただけではありません。血管とリンパ管の独立性という生命にとって基本的で重要な現象の分子基盤を明らかにしたという点で、医学・生物学の基礎研究における大きなブレークスルーとなりました。
分子レベルで解き明かされた精密な制御メカニズム
最新研究では、FLCNがどのようにして血管とリンパ管の独立性を維持するメカニズムを実現しているのか、分子レベルでの詳細な解明が行われました。この制御機構は、複数のタンパク質が連携して働く非常に精密なシステムです。
通常の状態では、FLCNというタンパク質がTFE3という転写因子を細胞質に留めておくことで、静脈におけるProx1という遺伝子の発現を抑制しています。Prox1は「リンパ管マスター転写因子」とも呼ばれる重要な遺伝子で、リンパ管内皮細胞のマーカーとして知られています。この遺伝子が静脈で発現すると、静脈内皮細胞がリンパ管様の性質を持つようになってしまいます。
しかし、FLCNが失われると、このバランスが崩れます。TFE3が核内に移行し、Prox1の発現が誘導されてしまうのです。その結果、静脈内皮細胞が「リンパ管様静脈内皮細胞」となり、血管とリンパ管の境界が曖昧になってしまいます。このような状態では、本来独立しているべき二つの系統が異常に接続してしまい、正常な生理機能が維持できなくなります。
TFE3という転写因子は、MiTF/TFEファミリーに属し、細胞のエネルギー状態や栄養状態に応じて様々な遺伝子の発現を制御する重要な分子です。通常は細胞質に局在していますが、特定のシグナルに応じて核内に移行し、標的遺伝子の転写を活性化します。FLCNはこのTFE3の細胞質局在を維持する役割を担っており、この制御機構が血管とリンパ管の分離維持のメカニズムにおいて極めて重要であることが、今回の研究により解明されました。
このような分子レベルでのメカニズムの解明は、基礎科学としての意義だけでなく、将来的な治療法開発への重要な手がかりを提供しています。FLCN-TFE3-Prox1という分子経路を標的とした薬剤開発により、血管とリンパ管の独立性を人為的に制御できる可能性が開けたのです。
リンパ浮腫治療への革新的応用可能性
血管とリンパ管の独立性維持メカニズムの解明は、リンパ浮腫という深刻な疾患の治療に新たな希望をもたらしています。リンパ浮腫は、リンパ管の機能不全によってリンパ液が組織内に溜まり、手足などが腫れてしまう病気です。特にがん治療後のリンパ節郭清や放射線治療の後遺症として発症することが多く、患者さんの生活の質を大きく低下させる深刻な問題となっています。
現在のリンパ浮腫の治療法は、主に圧迫療法やマッサージなどの保存的治療に限られており、根本的な治療法は確立されていません。患者さんは毎日弾性ストッキングを着用したり、専門的なリンパドレナージュマッサージを受けたりする必要があり、これらの治療は症状の緩和には役立ちますが、完治は困難です。
しかし、今回解明されたメカニズムを応用すれば、まったく新しいアプローチが可能になるかもしれません。具体的には、薬理学的にFLCNやTFE3の活性を制御することで、血管とリンパ管の間に制御された短絡路を作り出し、滞留したリンパ液を静脈系に排出させることが考えられます。これは従来の対症療法とは異なる、根本的な治療法となる可能性を秘めています。
このような治療法の実現には、局所的かつ可逆的に血管とリンパ管の独立性を調節する技術の開発が必要です。全身的にこのメカニズムを阻害してしまうと、正常な部位でも血管とリンパ管の異常な接続が起こってしまう可能性があるためです。局所投与可能な薬剤や、標的組織に選択的に作用する薬剤の開発が、今後の研究の重要な課題となります。
また、治療効果の持続時間や安全性の検証も重要です。一時的に短絡路を作ることで滞留したリンパ液を排出した後、再びしっかりと独立性が回復する必要があります。動物実験での有効性と安全性の確認を経て、最終的には臨床試験により人での効果を検証していく必要があります。このプロセスには時間がかかりますが、最新研究により明らかになったメカニズムは、リンパ浮腫に苦しむ多くの患者さんに希望をもたらすものとなっています。
血管とリンパ管の構造的・機能的違いとその意義
血管とリンパ管は、ともに内皮細胞から構成される管状構造を持っていますが、その構造や機能には重要な違いがあります。これらの違いを理解することは、両者の独立性維持のメカニズムを深く理解する上で不可欠です。
血管系は心臓という強力なポンプによって循環が維持されています。動脈は高い血圧に耐えるため、厚い筋層を持ち、弾性に富んだ構造をしています。毛細血管では血液成分の交換が行われますが、その壁は比較的密な構造を持ち、血液成分が不必要に漏れ出さないようになっています。毛細血管の外側にはコラーゲンなどのタンパク質で構成される基底膜が存在し、さらにペリサイトと呼ばれる裏打ち細胞が血管を補強しています。
一方、リンパ管系は心臓のようなポンプを持たず、筋肉の収縮や呼吸運動などによる外部からの圧力によってリンパ液が流れています。毛細リンパ管は片方が閉じた盲端構造を持ち、内皮細胞間の接着が緩く、組織液を容易に取り込めるようになっています。末梢のリンパ管、特に毛細リンパ管では、明瞭な基底膜やペリサイトが欠如しているか、あっても非常に薄く不連続です。この構造的特徴により、リンパ管内皮細胞は血管内皮細胞と比較して緊密に連結されておらず、毛細リンパ管の透過性は高くなっています。
この高い透過性こそが、組織液や大きな分子、さらには細胞をも取り込むことができるリンパ管の機能的特徴を生み出しています。リンパ管は老廃物や余分な水分の回収だけでなく、腸管からの脂肪の吸収や、免疫細胞の運搬という重要な役割も担っています。小腸の絨毛内にあるリンパ管(乳び管)は、食事由来の脂肪を含むカイロミクロンを吸収し、血液循環系へと運搬します。また、リンパ管は抗原や抗原提示細胞をリンパ節へと運び、リンパ節で活性化されたリンパ球を全身に分配する重要な経路となっています。
これらの構造的・機能的な違いを生み出す分子メカニズムの解明は、血管とリンパ管の独立性維持のメカニズム解明と密接に関連しています。最新研究で明らかになったFLCN-TFE3-Prox1経路は、まさにこのような違いを生み出すための遺伝子発現制御機構の一部なのです。
発生学的観点から見る血管とリンパ管の関係性
血管とリンパ管の関係を深く理解するためには、発生学的な観点からのアプローチが重要です。これら二つの系統がどのように形成され、どのようにして独立性を獲得するのかという過程を知ることで、成体における独立性維持のメカニズムがより明確になります。
発生学的には、血管とリンパ管は異なる起源から発生します。血管系は初期胚において血島と呼ばれる構造から形成され始めます。受精後間もない時期から、血管前駆細胞が集まって原始的な血管ネットワークが形成され、やがて心臓の形成と拍動の開始とともに、本格的な血液循環が始まります。
一方、リンパ管系は静脈の一部から分化して形成されます。この発生過程において、静脈内皮細胞の一部がリンパ管運命を獲得し、既存の静脈系から出芽してリンパ管ネットワークを形成していきます。最近の研究により、リンパ管前駆細胞は主静脈の底部にある多能性血管芽細胞集団から生じることが明らかになりました。この細胞集団は非常に興味深い性質を持っており、リンパ管だけでなく、動脈や静脈となる細胞系譜も生み出す能力を持っています。
このリンパ管運命決定において中心的な役割を果たすのが、先述のProx1という転写因子です。発生段階では特定の静脈内皮細胞でProx1が発現し、リンパ管が形成されますが、成体では静脈でのProx1発現は抑制される必要があります。FLCNはまさにこの抑制機構において重要な役割を果たしていることが、最新研究により解明されました。
発生段階でリンパ管が形成された後も、血管とリンパ管の独立性は厳密に維持される必要があります。もし成体になってから静脈でProx1が異常に発現してしまうと、血管とリンパ管の境界が曖昧になり、両者の正常な機能が損なわれてしまいます。FLCN-TFE3-Prox1経路による制御は、このような異常を防ぎ、生涯にわたって血管とリンパ管の独立性を維持するメカニズムとして機能しているのです。
がんにおける血管新生とリンパ管新生の複雑な関係
血管とリンパ管の独立性という観点は、がん研究においても極めて重要な意味を持っています。がん組織では、正常組織とは異なる複雑な血管とリンパ管のネットワークが形成され、これががんの進展や転移に深く関わっています。
固形がんは、ある程度の大きさまで成長すると、自身の代謝需要を満たすために新しい血管を形成する必要が生じます。がん細胞は、血管新生因子を分泌することで周囲の血管内皮細胞を刺激し、がん組織に向かって新しい血管を伸ばさせます。腫瘍が直径1〜2ミリメートル程度に達すると、がん細胞は酸素不足の状態に陥り、この低酸素状態に応答して、がん細胞はVEGF(血管内皮増殖因子)やFGF(線維芽細胞増殖因子)などの血管新生因子を大量に分泌します。
同時に、多くのがんではリンパ管新生も誘導されます。VEGF-C(血管内皮増殖因子C)やVEGF-D(血管内皮増殖因子D)などのリンパ管新生因子が発現し、これらがリンパ管内皮細胞のVEGFR-3(血管内皮増殖因子受容体3)に結合することでリンパ管新生が誘導されます。がん組織周囲や内部に形成された新生リンパ管は、がん細胞が所属リンパ節に転移する主要な経路となります。
興味深いことに、がん組織に形成される新生血管は、正常な血管とは異なる特徴を持っています。がん血管は構造的に未熟で、内皮細胞間の結合が緩く、基底膜も不完全です。そのため、血管からの漏出が起こりやすく、がん組織内の間質圧が上昇します。このような血管とリンパ管の異常な状態は、抗がん剤の腫瘍内への到達を妨げる要因ともなっています。
最新研究で解明された血管とリンパ管の独立性維持メカニズムは、がん組織における異常な血管・リンパ管形成の理解にも貢献する可能性があります。がん組織では、正常組織における独立性維持のメカニズムが破綻している可能性があり、このことが異常な血管・リンパ管ネットワークの形成に関与しているかもしれません。FLCN-TFE3-Prox1経路の異常ががん進展に関与しているかどうかについては、今後の研究が待たれるところです。
血管新生を標的とした抗がん治療は、すでに臨床で広く用いられています。ベバシズマブ(商品名:アバスチン)は、VEGFに結合してその作用を中和するヒト化モノクローナル抗体で、大腸がん、肺がん、腎がん、卵巣がんなど、多くのがん種において標準治療の一部として使用されています。しかし、リンパ管新生を標的とした治療法は、血管新生阻害療法ほど確立されておらず、今後の研究開発が期待される分野です。
オルガノイド技術の進展と血管・リンパ管研究への応用
血管とリンパ管のメカニズム研究において、近年注目されているのがオルガノイド技術です。オルガノイドとは、幹細胞から作製される三次元的なミニ臓器のことで、生体内の臓器の構造や機能を模倣した培養系です。この技術の進展により、血管やリンパ管を含む複雑な組織構造を試験管内で再現し、その形成メカニズムや機能を詳細に解析することが可能になってきています。
2024年11月には、理化学研究所が日本医療研究開発機構の支援を受けて、腎臓オルガノイドの成熟化を加速させることに成功したことが報告されました。また、東京科学大学(2024年10月に東京医科歯科大学と東京工業大学が統合して設立)では、iPS細胞から管腔組織を持つ腸を再現することに世界で初めて成功しています。このような管腔構造を持つオルガノイドは、血管やリンパ管のような管状構造を研究する上でも有用なモデルとなります。
オルガノイド技術は、血管やリンパ管の発生過程を詳細に解析したり、疾患モデルを作製したりすることを可能にします。例えば、FLCNを欠損させた細胞からオルガノイドを作製することで、血管とリンパ管の独立性が失われる過程を三次元培養系で観察することができます。このようなアプローチは、動物実験だけでは観察が難しい詳細な細胞挙動や分子動態を明らかにする上で有用です。
また、オルガノイドを用いた薬剤スクリーニングにより、血管とリンパ管の独立性を制御する新しい薬剤の開発を加速させることができます。FLCN-TFE3-Prox1経路を標的とする化合物のライブラリーをオルガノイドに適用し、血管とリンパ管の分離や接続を制御できる薬剤候補を効率的に探索することが可能になります。
顕微鏡イメージング技術とオルガノイド技術を組み合わせることで、三次元培養系における細胞の挙動や組織構造の変化を定量的に解析することが可能となり、より精密な研究が実現しつつあります。二光子顕微鏡や光シート顕微鏡などの高度な顕微鏡技術を用いることで、生きたオルガノイドの深部まで観察し、血管やリンパ管の形成過程をリアルタイムで追跡することができます。
再生医療における血管・リンパ管研究の重要性
血管とリンパ管のメカニズムに関する最新研究の成果は、再生医療の分野においても大きな意義を持っています。臓器移植や組織再生においては、移植した組織に血管やリンパ管を速やかに形成させることが成功の鍵となります。
2022年には東京医科歯科大学(現・東京科学大学)のグループが、世界で初めて自家腸上皮オルガノイドを潰瘍性大腸炎患者に移植する臨床研究を実施しました。このような再生医療の実現には、移植した組織が生着するための血管やリンパ管の形成が不可欠であり、血管・リンパ管研究の基礎知見が臨床応用に直結する好例となっています。
移植された組織が生着するためには、速やかに血管が形成されて酸素と栄養素の供給が確保される必要があります。同時に、組織から老廃物や余分な水分を排出するためのリンパ管の形成も重要です。これらの管状構造が適切に形成され、かつ独立性を保って機能することが、移植組織の長期的な生存と機能維持に不可欠なのです。
血管新生やリンパ管新生のメカニズムを理解し、これを人工的に制御する技術が開発されれば、再生医療の成功率を大きく向上させることができます。例えば、移植する組織に対して適切な血管新生因子やリンパ管新生因子を添加したり、FLCNなどの独立性維持に関わる分子の発現を調節したりすることで、理想的な血管とリンパ管のネットワークを形成させることが可能になるかもしれません。
大日本印刷は2025年度に向けて「ミニ腸」の量産化プロセスの開発を進めており、再生医療や創薬への応用が期待されています。このような三次元培養組織の量産化技術が確立されれば、血管やリンパ管を含む複雑な組織構造を持つオルガノイドの産業応用が加速し、創薬や再生医療の分野に大きな変革をもたらす可能性があります。
脳リンパ管の発見と神経疾患への新たな視点
血管とリンパ管の研究において、近年特に注目されているのが脳におけるリンパ管の発見です。脳は長い間「リンパ管のない臓器」と考えられてきましたが、最近の研究により、脳を覆う硬膜にリンパ管が存在することが発見されました。この発見は、脳の老廃物除去システムや神経変性疾患の理解に新たな視点をもたらしています。
硬膜リンパ管は脳脊髄液や間質液の排出に関与しており、脳の老廃物除去システムにおいて重要な役割を果たしていると考えられています。さらに注目すべきことに、硬膜リンパ管の機能不全がアルツハイマー病や脳血管障害などの神経変性疾患に関与している可能性が示唆されています。
アルツハイマー病では、アミロイドβなどの異常タンパク質が脳内に蓄積することが病態の中心にあると考えられていますが、これらの異常タンパク質の排出に硬膜リンパ管が関与している可能性があります。実際、動物実験では、硬膜リンパ管の機能を改善することで認知機能が向上する例も報告されており、この分野の研究は急速に進展しています。
脳における血管とリンパ管の独立性やその相互作用についても、今後の研究で明らかにされていくべき重要な課題です。硬膜リンパ管においても、FLCN-TFE3-Prox1経路が独立性維持に関与しているのか、あるいは脳特有の別のメカニズムが存在するのかについては、さらなる解明が待たれます。
緑内障についても、最近の研究でリンパ管との関連が指摘されています。緑内障は眼圧上昇により視神経が障害される疾患で、眼球周囲のリンパ管が房水(眼内を満たす液体)の排出に関与している可能性が示唆されており、リンパ管の機能改善が新たな治療戦略となる可能性が検討されています。
今後の研究展望と医療への応用可能性
血管とリンパ管の独立性維持メカニズムの解明から始まった研究は、今後さらに広範な医療分野への応用が期待されています。FLCN-TFE3-Prox1経路以外にも、血管とリンパ管の独立性維持に関わる分子機構が存在する可能性があります。複数の制御機構が協調的に働くことで、より強固な独立性維持が実現されているのかもしれません。
また、発生段階と成体では制御メカニズムが異なる可能性もあり、時期特異的な制御メカニズムの解明も重要な課題です。発生段階では静脈の一部からリンパ管が分化する必要があるため、Prox1の発現が積極的に誘導されますが、成体では逆にこの発現を抑制する必要があります。FLCNはこの成体における抑制機構の一部ですが、発生段階でのProx1発現誘導メカニズムについても、さらなる研究が必要です。
実際の治療への応用を考えると、FLCNやTFE3の活性を薬理学的に制御する化合物の開発が重要となります。リンパ浮腫の患者さんに対して、局所的にこれらの分子の機能を調節することで、静脈とリンパ管の間に制御された吻合を誘導し、滞留したリンパ液を排出させる治療法が実現できるかもしれません。ただし、このような治療法の開発には、安全性や有効性の慎重な検証が必要です。
がん治療への応用も期待されます。がん組織における血管とリンパ管の異常なネットワーク形成に、FLCN-TFE3-Prox1経路の異常が関与しているかを明らかにすることで、新たな治療標的が見つかる可能性があります。特に、リンパ管新生を標的とした治療法の開発は、がんのリンパ節転移を防ぐ上で重要な戦略となり得ます。
最新研究により明らかになった血管とリンパ管の独立性維持メカニズムは、基礎科学としての意義だけでなく、リンパ浮腫治療、がん治療、神経変性疾患治療、さらには再生医療やオルガノイド創薬まで、幅広い医療分野への応用が期待されています。基礎研究で得られた知見が臨床応用へと発展し、最終的には患者さんの利益につながることこそが、医学研究の究極の目標です。今後も、血管とリンパ管の関係性についての理解が深まり、新たな治療法の開発が進展することが期待されます。熊本大学と慶應義塾大学の研究チームによる画期的な発見は、この分野における重要なマイルストーンとなり、今後数十年にわたる研究と医療応用の礎となるでしょう。








コメント